Tip van de maand
nuttige wenken en praktische tips voor de mineralenverzamelaarvoor vragen of suggesties, email tips@minerant.org
Tip 77: microchemie deel 16: aluminium (Al3+) aantonen
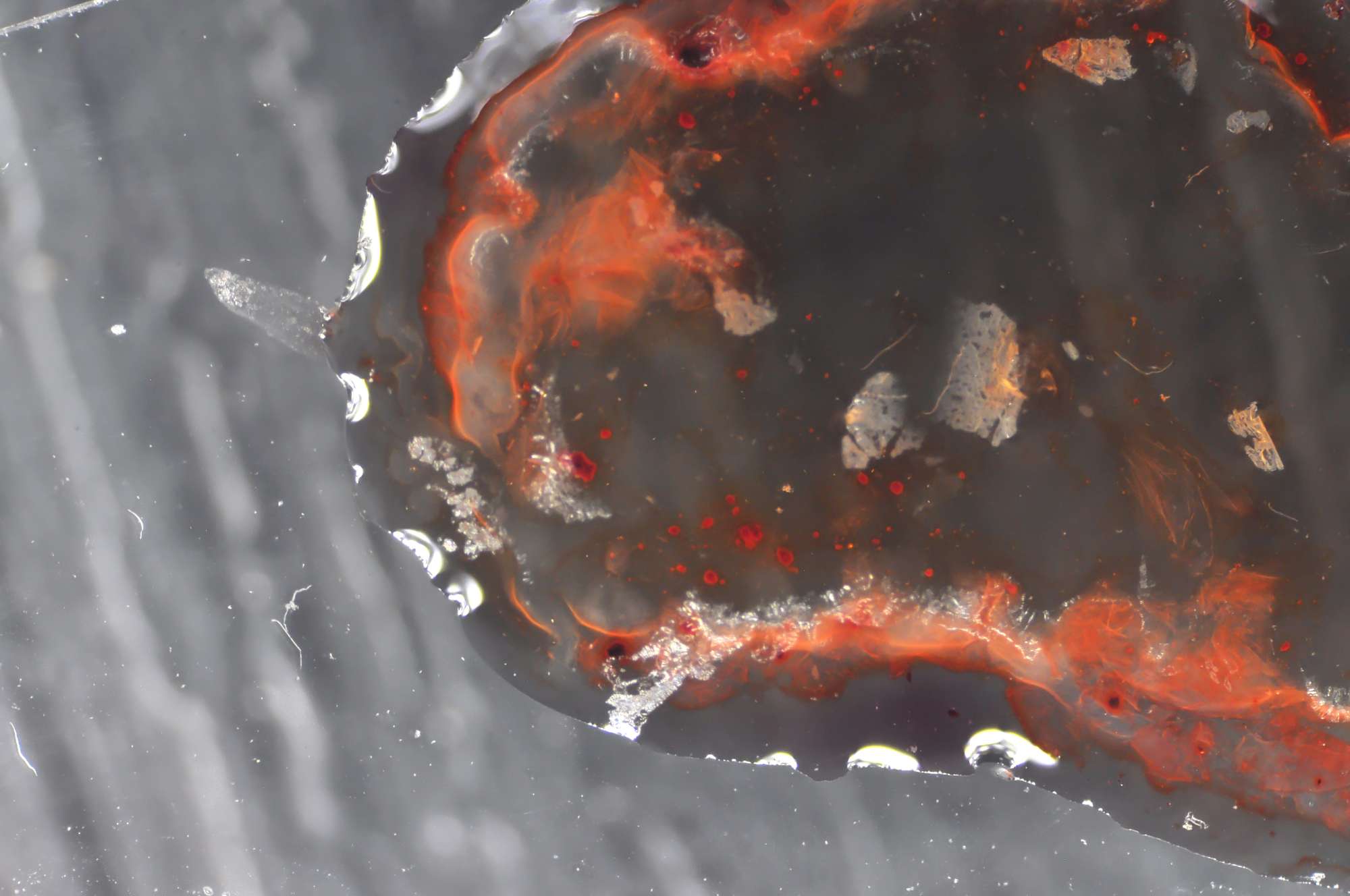
Roodkleuring van aluminiumhydroxide door alizarine-S. Beeldbreedte ruim 1 cm.
Er zijn volgens mindat (oktober 2022) 1179 mineralen die het element aluminium bevatten. Meer dan de helft daarvan (629 stuks) zijn silicaten. Daarin is het element aluminium meestal niet aan te tonen met microchemisch onderzoek. Bij de andere 550 zitten er veel die in water, zuur of base op te lossen zijn en dus wel microchemisch onderzocht kunnen worden. Te denken valt hierbij aan sulfaten, carbonaten, fosfaten en arsenaten. Een van de meest bekende, korund, Al2O3 (robijn, saffier), hoort daar niet bij.
Op mineralenbeurzen worden vaak mooie, goed gevormde octaëdervormige kristallen aangeboden die kleurloos of lichtpaars zijn. Het gaat dan vaak om synthetische kristallen van aluin ( KAl(SO4)2·12H2O ). De paarse kleur ontstaat als een beetje van het aanwezige Al vervangen is door chroom (Cr).
Aan kunnen tonen of aluminium aanwezig is, is dus zinvol en gelukkig ook vrij eenvoudig.
Voorbereiding:
Van het te onderzoeken materiaal (mineraal) moet een oplossing gemaakt worden waarin het aluminium aangetoond kan worden.
Soms (zoals bij aluin) kan dat door domweg een beetje (uiteraard gedemineraliseerd) water toe te voegen. Bij slecht oplosbare mineralen (zoals fosfaten en arsenaten) is meestal wat zoutzuur nodig. Aangezien voor de test een neutrale oplossing gewenst is, moet het overschot zoutzuur weggenomen worden. Het gemakkelijkst is het dan in te dampen en aan het residu water toe te voegen.
De test:
- Leg een druppel van de te onderzoeken vloeistof op een microscopeerglaasje op de houder daarvoor (zie tip 3).
- Leg daarnaast een speldenkop-grote hoeveelheid alizarine-S.
- Voeg daaraan een druppel ammonia (10%) toe, zodat een paarse oplossing ontstaat.
- Meng dan de beide druppels.
Al3+ + 3 OH- → Al(OH)3
Dat neerslag kleurt meteen rood door de alizarine-S.
Hoe dat er uit kan zien toont de foto hierboven.
Opmerking:
Schuster (lit. 2) beschrijft de test met natronloog in plaats van ammonia. Bij die werkwijze bestaat het risico dat een te hoge concentratie loog het aluminiumhydroxide oplost en de rode kleur uitblijft.
Het oplossen van het aluminiumhydroxide door overmaat loog, ook vereenvoudigd:
Al(OH)3 + 3 OH- → Al(OH)63-
Tot slot nog de altijd geldende opmerkingen:
1. Vergeet niet de nodige voorzorgsmaatregelen nemen om verantwoord en veilig te werken!
2. Begin met “waardeloos” rest-materiaal.
3. Test altijd ook met bekende mineralen om te kunnen vergelijken met de waarnemingen bij het te onderzoeken mineraal.
Literatuur:
1. Demaret Cristian: Microchimie, appliquée à la détermination de minéraux par voie humide, Cercle Geologique de Hainaut, 2017
2. Norbert Schuster: Mineralbestimmung durch einfache chemische und physikalische Methoden, Christian Weise Verlag, München, 2007, ISBN 978-921656-69-3.
